Yuling CHEN soutiendra sa thèse réalisée au Laboratoire des applications Thérapeutiques des Ultrasons (LabTAU) et au Laboratoire de Mécanique des Fluides et d'Acoustique (LMFA) le 14 mars 2025 à 10h30 dans la salle de conférence du LabTAU (Lyon) et par visioconférence.
Titre : Endofibrose artérielle iliaque : analyse des contraintes pariétales dans une conduite coudée et faisabilité d’un traitement par ultrasons focalisés.
Encadrement : Jean-Christophe Béra, Thomas Castelain, Xavier Escriva, Bruno Gilles.
Résumé :
L’endofibrose artérielle (EA) iliaque externe est une maladie vasculaire non-athéromateuse spécifique du sportif. 90% des patients sont des cyclistes jeunes sans facteur de risque de maladie cardiovasculaire traditionnelle.
L'EA est une lésion sténosante paucicellulaire, caractérisée par un épaississement de la paroi artérielle et une réduction subséquente de sa lumière, générant un apport sanguin défectueux aux membres inférieurs des athlètes.
Le seul traitement actuel si le patient souhaite continuer son activité est chirurgical, et consiste à réaliser une endofibrosectomie.
Bien que diverses hypothèses étiologiques aient été avancées, aucune étude spécifique n'a encore testé ces hypothèses sur des expériences in vitro, in vivo ou in silico. Ce travail est consacré à l’hypothèse selon laquelle une contrainte de cisaillement pariétale (Wall Shear Stress, WSS) excessive due à la surcourbure de l’artère pourrait être à l’origine du développement de l’EA.
Pour étudier cette hypothèse, un modèle très simplifié d’écoulement d’artère iliaque externe sans présence de sténose est adopté : écoulement newtonien dans une conduite cylindrique rigide de rayon R avec une courbure unique, qui est caractérisée par un rayon de courbure (Rc), un ratio de courbure (δ=R/Rc) et un angle d’ouverture (θo). Pour une première approche, nous nous concentrons sur l’étude en régime permanent, en préparation de futures recherches en régime pulsé.
Deux approches expérimentale et numérique ont été développées pour analyser l’effet de la géométrie du coude sur l'amplitude et la localisation de WSS.
Un modèle numérique est développé avec le logiciel CFD OpenFOAM® et un modèle expérimental est conçu basé sur vélocimétrie Laser Doppler.
La comparaison entre les résultats des profils de vitesse axiale et des estimations de WSS axial numériques et expérimentaux, dans les configurations suivantes : δ =1/6, θo =55° et 90°, Re = 550 et 2200, fournit une validation croisée.
Une étude paramétrique numérique est ensuite menée, basée sur les grandeurs δ = [1/10,1/2], θo = [25°,180°] et Re = [275,2720].
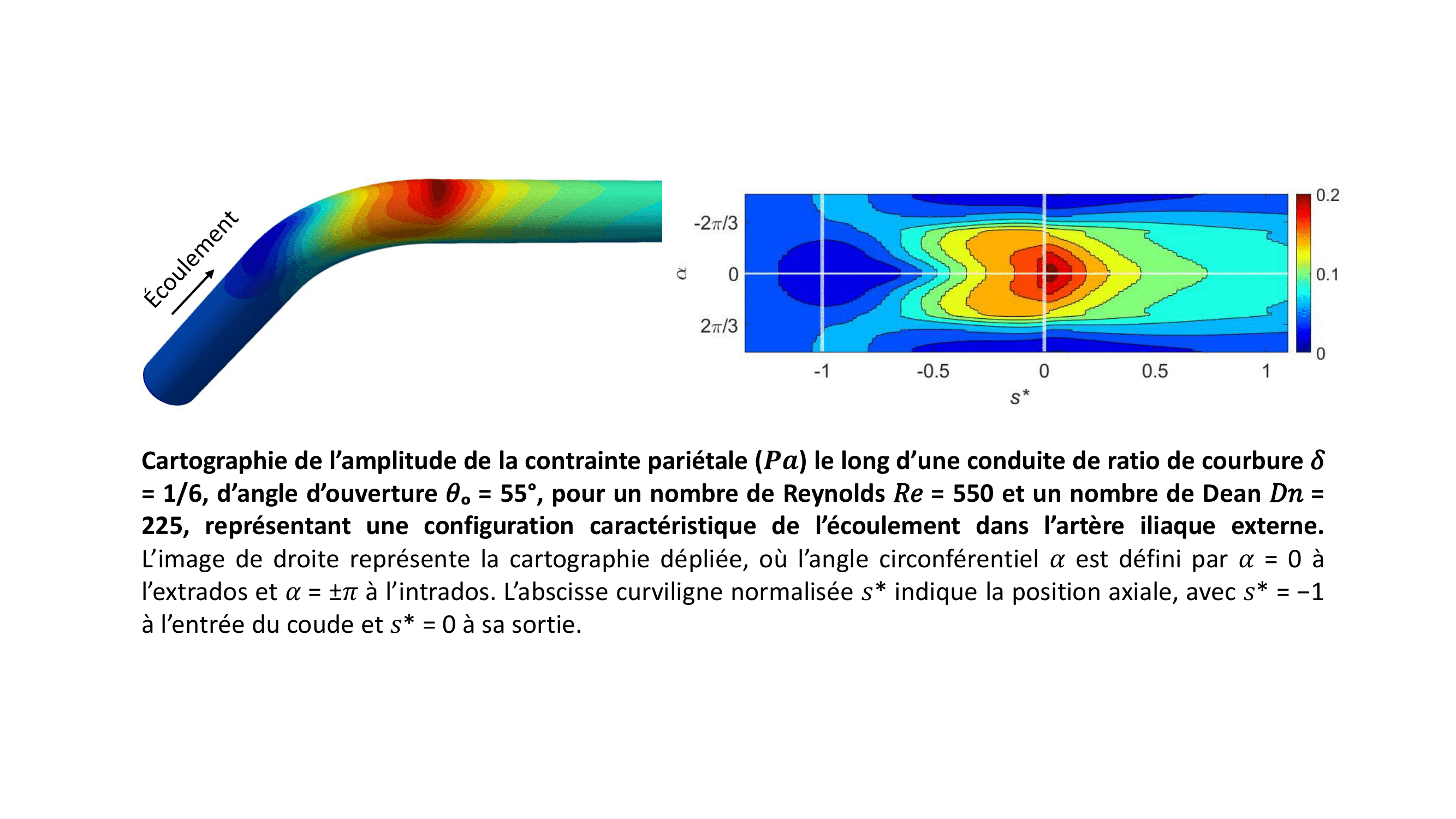
L’étude révèle que la composante axiale (WSS1) est dominante, et il existe deux zones de WSS1 extrémal si l’écoulement dans le coude est complètement développé. La valeur maximale de WSS1 est atteinte toujours à la sortie du coude, indépendamment de δ, θo et Re. En revanche, la position du second maximum est fonction de la racine du ratio de courbure (√δ). Les valeurs de ces deux maximums sont fonction de la racine du nombre de Dean (√(Re √δ )). D'autre part, dans le cas d’un écoulement non développé dans une conduite coudée courte, correspondant généralement aux cas de l’artère iliaque, une seule zone de WSS1 extrémal existe, toujours à la sortie du coude, et sa valeur est plus importante que pour un écoulement de Dean développé.
Nous avons ainsi identifié des configurations défavorables pour l'artère, i.e. écoulements de Dean non développés, pour lesquelles la surcontrainte est la plus significative.
En parallèle, en vue d’investiguer la possibilité d’un traitement par ultrasons, un objectif secondaire du travail porte sur la faisabilité de la destruction d’un fragment d’EA par cavitation ultrasonore focalisée. Une étude expérimentale sur des échantillons de tissus prélevés en per-opératoire sur des patients fournit des résultats qualitatifs encourageants.
Lien visio : Contacter



