Par F. Khannous.
La dissection aortique est une pathologie vasculaire qui consiste en la fissuration de la couche interne de la paroi aortique et l’infiltration du sang à l’intérieur formant ainsi un deuxième chenal de circulation sanguine appelé faux chenal. Les deux chenaux sont séparés par la paroi disséquée appelé flap néointimal.
Les dissections sont généralement classifiées en deux types. Le type A (DATA), la fissuration se situe sur le segment ascendant de l’aorte thoracique et peut s’étendre au segment descendant ; le type B (DATB) la fissuration se situe sur le segment descendant. Une DATA est traitée chirurgicalement par la pose d’une prothèse sur le segment ascendant. Une dissection résiduelle peut persister dans le segment descendant, on l’appelle une DATB résiduelle. Elle est prise en charge comme les autres DATB, par un traitement médicamenteux, mais dans plus de 30% des cas elle évolue défavorablement ce qui nécessite une nouvelle intervention.
Actuellement, il est encore difficile de prédire précocement cette évolution en utilisant seulement des critères cliniques. Face à ce constat, notre objectif est d’identifier des paramètres biomécaniques prédictifs de l’évolution des DATBR à travers la modélisation et la caractérisation de l’hémodynamique dans ce contexte pathologique.
Des simulations numériques patient-spécifique et tenant compte des interactions fluide structure sont développées pour deux cas de patients ayant évolué avec et sans complications (cas défavorable versus favorable) et pour deux temps de suivi post-opératoire correspondant à la pose de la prothèse (T0) et 12 mois après (T1). Les morphologies sont reconstruites à partir d’imagerie médicale. En entrée, les profils de vitesses sont issus d’un débit enregistré au niveau de l’aorte ascendante. Des modèles Windkessel à 3 éléments sont définis à chaque sortie afin de reproduire des pressions physiologiques mimant l’effet du traitement médicamenteux anti-hypertensif. Les paramètres de chaque Windkessel sont estimés à travers une procédure d’optimisation sous contraintes alliant un algorithme génétique et des simulations numériques. Le comportement rhéofluidifiant du sang et la déformabilité des structures sont pris en considération.
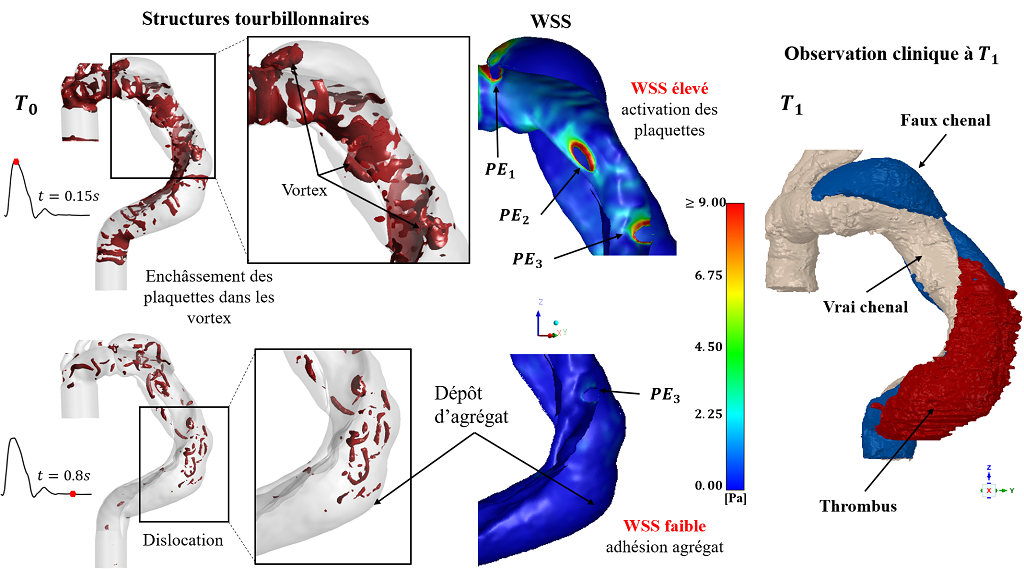
Cas défavorable : rôle de la dynamique des structures tourbillonnaires et de la distribution du WSS à T0 dans la formation de thrombus à T1. PEi : Porte d’entrée.
L’analyse comparative de l’hémodynamique des deux cas de patients aux deux temps de suivi a notamment permis d’établir des liens entre des index biomécaniques et des évènements cliniques délétères observés à (T1). Le rôle combiné de la distribution du WSS et de la dynamique des structures vorticales dans la formation et le développement d’un thrombus (Figure ci-dessus) a ainsi été mis en évidence. Les forts WSS présent au niveau des portes d’entrée générées par les fissurations provoquent l’activation des plaquettes qui forment alors des agrégats qui sont par la suite transportés par les structures vorticales dans le faux chenal distal. A la fin du cycle, la dislocation des vortex engendre le relargage des agrégats qui adhèrent en paroi en des zones de faible WSS débutant la formation de thrombus. Ces mécanismes sont confirmés par les observations cliniques faites à T1.
Grâce à cette meilleure compréhension du rôle de chaque paramètre biomécanique dans l’évolution de la pathologie, il est possible de prédire et d’anticiper les potentielles complications cliniques dès les premiers mois de suivi.
Publications
F. Khannous, C. Guivier-Curien, M. Gaudry, P. Piquet & V. Deplano. Residual type B aortic dissection FSI modeling. Computer Methods in Biomechanics and Biomedical Engineering, 23:sup1, S153-S155 https://doi.org/10.1080/10255842.2020.1812165
Khannous, Fatma. (2020). Modélisation biomécanique et pathologies de l'aorte. Suivi clinique dans le contexte de la dissection aortique de type B résiduelle. [Thèse de doctorat, Aix-Marseille Université].
L’auteur

Fatma Khannous est Docteur d’Aix-Marseille Université en sciences pour l’ingénieur spécialité mécanique et physique des fluides depuis Septembre 2020. Sa thèse a été effectuée dans l'équipe de Biomécanique IRPHE, UMR7372, en collaboration avec le Centre Aorte de l’Hôpital la Timone à Marseille. Elle est également ingénieur en modélisation pour l’industrie et le service, spécialité calcul scientifique (Ecole Nationale d’Ingénieurs de Tunis, Tunisie).
Copyright
© 2020 par l’auteur. Sauf mention contraire, le contenu du blog de la Société de Biomécanique (texte et figures) est distribué sous licence Creative Commons Attribution - Partage dans les mêmes conditions 4.0.



