Par Beatrice Bisighini, prix de thèse de la SB 2025.
La rupture d’un anévrisme intracrânien provoque une hémorragie dans l’espace entourant le cerveau, une urgence médicale grave associée à un risque élevé de mortalité et nécessitant une prise en charge immédiate. Les techniques endovasculaires sont aujourd’hui le traitement de première intention, notamment la diversion de flux, qui consiste à implanter des stents à haute densité pour isoler le sac anévrismal et réduire l’afflux sanguin. Pour choisir le dispositif le plus adapté pour un patient, cette approche repose toutefois sur des mesures manuelles réalisées à partir d’images médicales, ce qui comporte un risque d’erreur susceptible d’entraîner des complications péri- ou postopératoires (Figure 1).
Les modèles computationnels peuvent devenir des outils précieux pour planifier les interventions endovasculaires, permettant d’explorer différentes options thérapeutiques et d’anticiper les risques. En particulier, la simulation par éléments finis (EF) constitue la méthode la plus précise pour reproduire le comportement de différents dispositifs médicaux en tenant compte de l’anatomie propre du patient (Auricchio et al., 2011; Ma et al., 2012; Perrin et al., 2015). Toutefois, l’urgence des interventions sur les anévrismes intracrâniens limite l’utilisation clinique de ces simulations, dont la complexité entraîne des temps de calcul trop longs (quelques heures). Cette thèse a exploré la faisabilité d’un outil capable de simuler en temps réel le déploiement de stents avec précision, en combinant simulations EF et apprentissage automatique (AA).
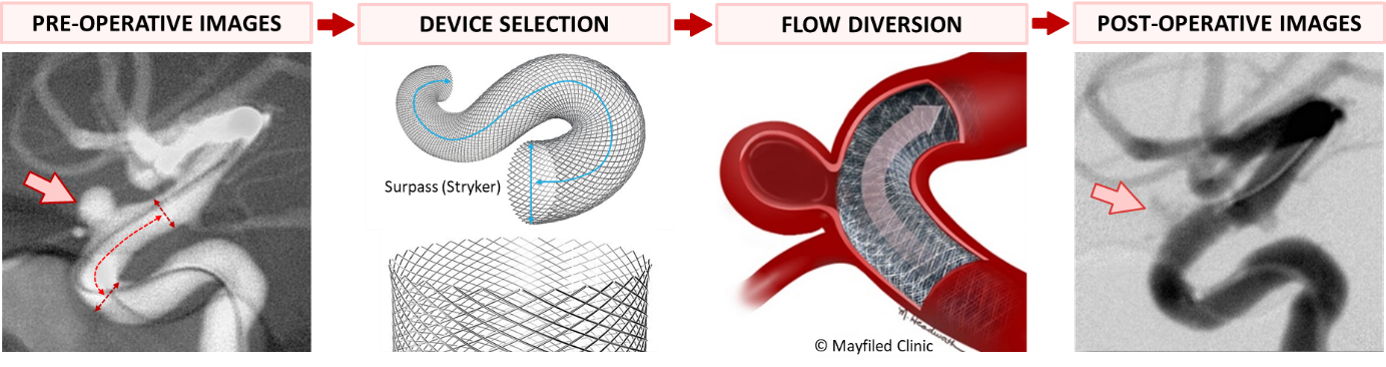
Figure 1
La première étape a consisté à développer EndoBeams.jl, un solveur EF open-source permettant de réaliser des simulations rapides de déploiement de stents (quelques dizaines de minutes). Les résultats du solveur ont été vérifiés à l’aide de tests de référence (benchmarks) issus de la littérature (Bisighini et al., 2022). Par la suite, une validation expérimentale a été menée à l’aide de tests de flexion trois points et d’essais de déploiement de stents dans des reproductions imprimées en 3D de vaisseaux carotidiens. Les simulations numériques ont montré une bonne cohérence avec les observations in vitro, tant sur les valeurs de force des tests de flexion que sur les images 2D et les micro-scans CT acquises pendant et après les essais (Figure 2, à gauche).
Dans un second temps, un modèle de forme statistique a été dérivé d’une base clinique comprenant 80 cas pour générer des artères cérébrales synthétiques supplémentaires reproduisant la variabilité anatomique observée. Dans cette étape, les anévrismes ont été retirés afin de simplifier la paramétrisation. Enfin, un modèle d’AA a été entrainé pour établir une correspondance entre les caractéristiques géométriques des artères synthétiques et la configuration du stent déployé. EndoBeams.jl a permis de réaliser ces simulations EF et générer rapidement de larges bases de données, indispensables à l’entraînement des modèles d’AA.
Les résultats obtenus sur de nouveaux cas ont été prometteurs, avec des erreurs de prédiction comparables à la résolution spatiale des images médicales (Bisighini et al., 2025). Cela a démontré la capacité de ces techniques à fournir des prédictions du déploiement de stents en quelques millisecondes, tout en conservant le réalisme mécanique et la fiabilité des simulations EF (Figure 2, à droite). Malgré les simplifications anatomiques (absence de collets d’anévrismes) et les hypothèses de modélisation (parois rigides pour les artères), cette étude reste représentative du contexte clinique et pourrait être étendue à des applications plus complexes sans modifications majeures.
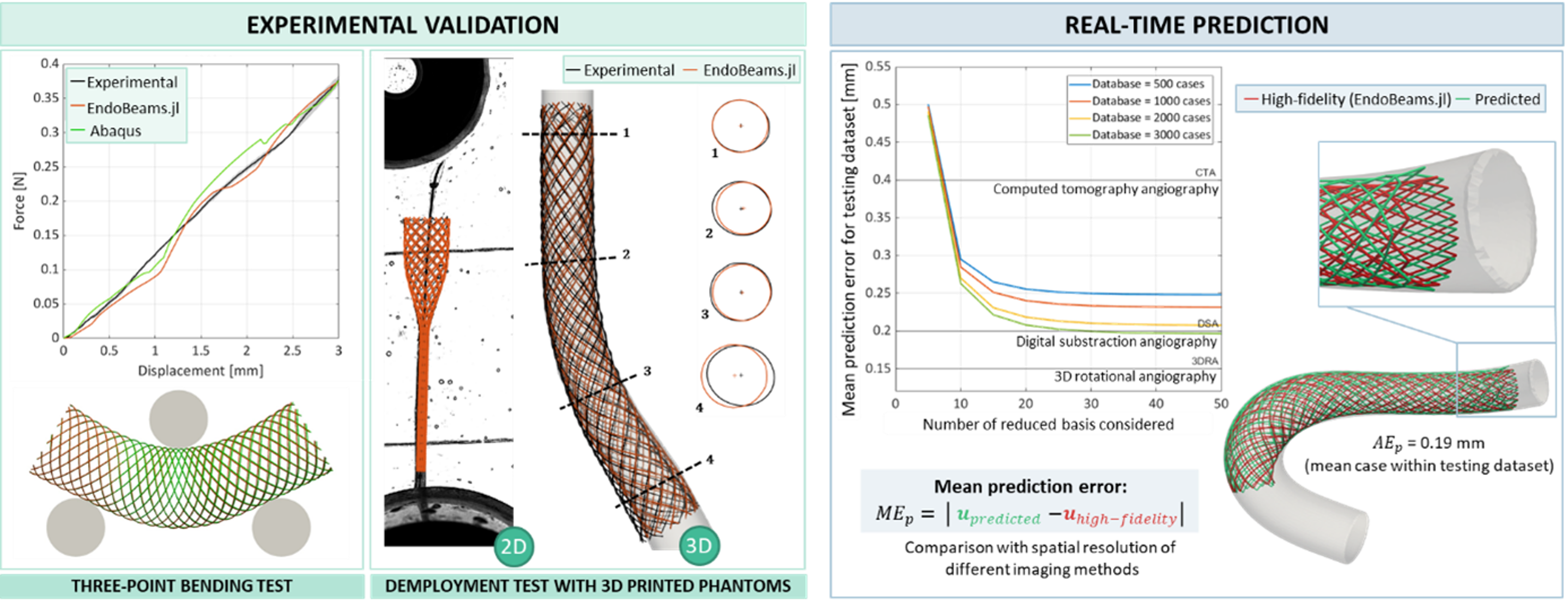
Figure 2
Références
Auricchio, F., Conti, M., De Beule, M., De Santis, G., & Verhegghe, B. (2011). Carotid artery stenting simulation: From patient-specific images to finite element analysis. Medical Engineering & Physics, 33(3), 281–289. https://doi.org/10.1016/j.medengphy.2010.10.011
Bisighini, B., Aguirre, M., Pierrat, B., & Avril, S. (2025). Machine learning and statistical shape modelling for real-time prediction of stent deployment in realistic anatomies. Computer Methods and Programs in Biomedicine, 260, 108583. https://doi.org/10.1016/j.cmpb.2024.108583
Bisighini, B., Aguirre, M., Pierrat, B., Perrin, D., & Avril, S. (2022). EndoBeams.jl: A Julia finite element package for beam-to-surface contact problems in cardiovascular mechanics. Advances in Engineering Software, 171, 103173. https://doi.org/10.1016/j.advengsoft.2022.103173
Ma, D., Dargush, G. F., Natarajan, S. K., Levy, E. I., Siddiqui, A. H., & Meng, H. (2012). Computer modeling of deployment and mechanical expansion of neurovascular flow diverter in patient-specific intracranial aneurysms. Journal of Biomechanics, 45(13), 2256–2263. https://doi.org/10.1016/j.jbiomech.2012.06.013
Perrin, D., Badel, P., Orgéas, L., Geindreau, C., Dumenil, A., Albertini, J.-N., & Avril, S. (2015). Patient-specific numerical simulation of stent-graft deployment: Validation on three clinical cases. Journal of Biomechanics, 48(10), 1868–1875. https://doi.org/10.1016/j.jbiomech.2015.04.031
L'auteure

Beatrice Bisighini, Mines Saint-Etienne
Beatrice Bisighini est actuellement chercheuse postdoctorale dans le cadre d’un projet collaboratif entre Mines Saint-Étienne et l’Université de Montpellier, où elle étudie le comportement mécanique des tissus périnéaux. Elle a soutenu son doctorat en février 2024 à Mines Saint-Étienne, portant sur le développement d’outils computationnels avancés pour les traitements endovasculaires.
Copyright
© 2025 par l’auteur. Sauf mention contraire, le contenu du blog de la Société de Biomécanique (texte et figures) est distribué sous licence Creative Commons Attribution - Partage dans les mêmes conditions 4.0.



